





.

Membresías
Miembro de: ASCO: American society for clinical oncology, www.asco.org
licación, aplicación de células o exosomas, aislamiento y concentración de células y exosomas, controles de calidad (viabilidad celular e inmunofenotipifación celular por citometría), estabilización y duración, liofilización, factor de compensación de principio activo, etc.






Cartas de Referencia
La inmunoterapia CD en cáncer
Importancia:
Cada día, son más los pacientes que quedan sin propuesta de tratamiento y son desahuciados o enviados solo a manejo paliativo. Sin embargo, el desarrollo de TERAPIAS AVANZADAS en Cáncer, abre nueva opción. Actualmente, el Cáncer es, en muchos países de Latinoamérica, 2ª o hasta 1ª causa de muerte, según región o provincia. La realidad refleja que es un problema

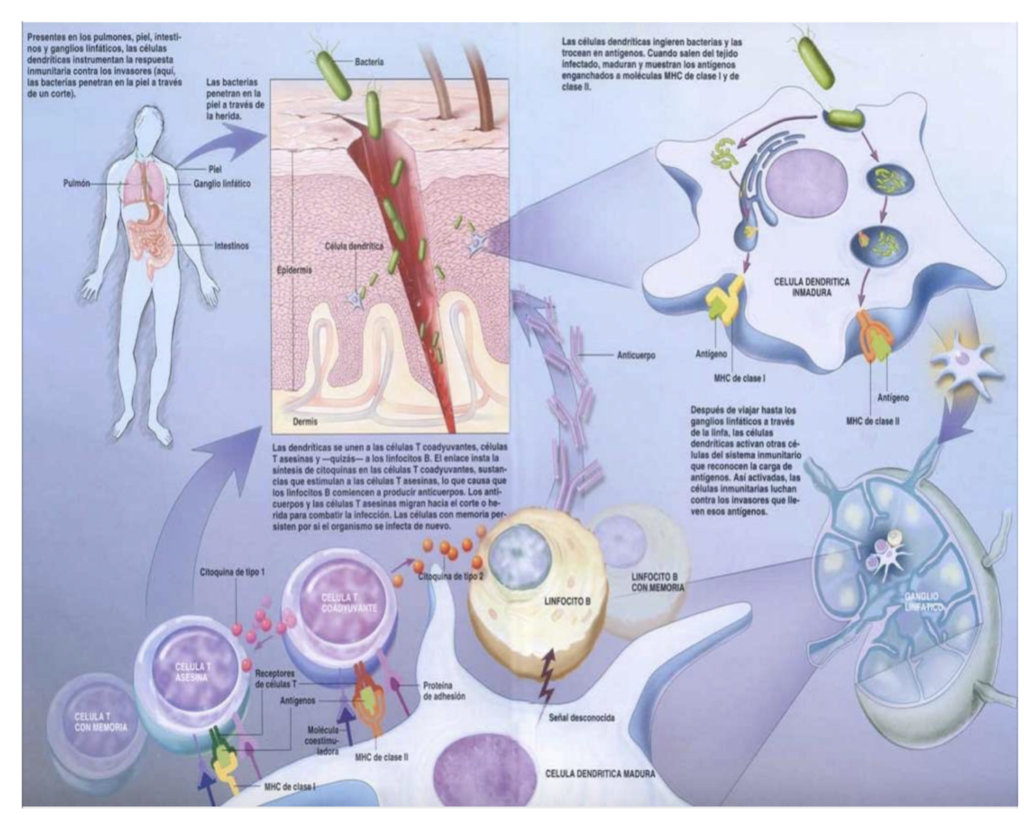
Sin embargo, los tratamientos convencionales son esenciales para el abordaje inmediato del cáncer y el intento por controlar el crecimiento de la masa tumoral. Recordemos que hasta hoy, no existe CURA garantizada conocida para el cáncer, y todas las propuestas de tratamiento buscan equilibrar factores como: acceso universal, costo a cargo del Estado o aseguradoras de salud, índice razonable de resultados variados (curación, estabilización de la enfermedad, remisión parcial, mantención de calidad de vida a pesar de progresión, aumento de expectativa de vida, potenciación de otras terapias (sinergia), etc.
Para quienes y cuando?:
En cualquier momento de su evolución del cancer: antes, durante o después de terapias convencionales. Para todo paciente cuando necesita URGENTE un TRATAMIENTO DE CANCER y ocurre una o más de las siguientes situaciones:
Para que tipo de cáncer?
En cualquier etapa de cáncer, con propósitos específicos para queda etapa. Efectiva para TUMOR SOLIDO (99% de los distintos cáncer) que incluye carcinoma (cáncer de mama, gástrico, colón, vesícula biliar, hepático, renal, testicular, ovárico, ginecológico, piel, próstata, páncreas, pulmón y otros), gliomas, sarcoma, melanoma, linfomas no hodgkin, entre otros y con variantes disponibles para Leucemias.
Por qué se requiere en Cáncer, la INMUNOTERAPIA del tipo ONCOVIX-ID ® ?
Sus Propósitos:
Un paciente bien informado entiende que la curación o remisión total es el resultado ideal de un tratamiento oncológico. Sin embargo, es sabido que ello no se obtiene en hasta el 50% de los pacientes atendidos por oncología convencional de cirugía, quimioterapia y radioterapia, que debe ser complementada y reforzada para mejorar ese porcentaje de respuesta favorable
La Inmunoterapia de DEXos acerca notablemente a los siguientes resultados, con o sin terapia convencional asociada:

Su Monitoreo:
Durante décadas,la acción de los tratamientos sistémicos y/o convencionales en oncología ha sido la destrucción de las células tumorales con mecanismos citotóxicos. Desafortunadamente, las células tumorales desarrollan resistencia. Sin embargo, a medida que se han ido conociendo mejor los mecanismos por los que se desarrollan las neoplasias, han ido surgiendo nuevos tratamientos basados en el sistema inmune. Para evitar esta resistencia se aplica lo que se denomina inmunoterapia activa, que utiliza el sistema inmune del paciente que puede, potencialmente, detectar y adaptarse a los cambios del tumor evitando que eluda al sistema inmune.
La inmunoterapia activa utiliza tanto la inmunidad humoral como la celular para luchar contra el tumor. Sus efectos pueden producir respuestas que no se manifiesten con disminución del tamaño y/o de la actividad metabólica, como lo hacían los tratamientos quimioterápicos tradicionales, mediante criterios RECIST (basados esencialmente número y tamaño de lesiones tumorales) Con la inmunoterapia activa en el tratamiento de tumores, se ha observado:
También, se observan tres NUEVOS patrones de respuesta, además de los observados habitualmente
CONTEXTO GUIA:

PET-CT. La técnica de Tomografía por Emisión de Positrones (PET, Positron Emission Tomography) fusionada con las imágenes obtenidas de una Tomografía com putada (CT), denominada (PET-CT), proporciona in formación de las alteraciones y de la actividad metabólica de las lesiones identificadas en estudio, proporcionado además una resolución espacial superior a aquellas que convencionalmente se obtienen con la CT. La evaluación de la actividad metabólica se determina a partir del índice semicuantitativo de captación del trazador, conocido como SUV (Standard Uptake Value), que se define como la cantidad de radiotrazador presente en una lesión según la dosis administrada, pudiéndose comparar este valor entre controles sucesivos, objetivando apreciaciones visuales. Interpretación de resultados [Immune-Modified Response Evaluation Criteria In Solid Tumors (imRECIST)
Su Evidencia: Detalles en,
)

Derecho a la información:Un PACIENTE de cáncer, posee derecho a conocer que la propuesta de tratamiento que reciba, puede estar condicionada por:

RESUMEN: DEXos – INMUNOTERAPIA DE CÉLULAS DENDRITICAS Y EXOSOMAS
Destacada en distintas publicaciones por ser 1 de las 3 inmunoterapias (junto a T-CAR e inhibidores de checkpoints) con mayor respaldo, así como alta precisión, personalizada, de mínimas reacciones adversas y de costo más accesible en comparación a otras inmunoterapias. Ver pág. 20, créditos a REVISTA: “Investigación y Ciencia, especial de INMUNOTERAPIA CONTRA EL CANCER, 2018”; https://www.investigacionyciencia.es/revistas/especial/inmunoterapia-contra-el-cncer-748
Referencias Bibliográficas
a. Steinman RM, Cohn ZA. Identification of a novel cell type in peripheral lymphoid organs of mice. I. Morphology, quantitation, tissue distribution. J Exp Med 1973;137(5): 1142-1162. Disponible en http://www.ncbi.nlm.nih.gov/ pmc/articles/PMC2139237/pdf/1142.pdf
b. Cheong C, Choi JH, Vitale L, He LZ, Trumpfheller C, Bozzacco L, et al. Improved cellular and humoral immune responses in vivo following targeting of HIV Gag to dendritic cells within human anti-human DEC205 monoclonal antibody. Blood 2010;116(19):3828-3838. Disponible en http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2981538/? tool=pubmed
c. Palucka AK, Paczesny S, Dhodapkar MV, Steinman RM, Fay JW, Banchereau J Dendritic cells as melanoma vaccines. J Invest Med 2003;51(Supl 2):S385-S386.
d. Banchereau J, Palucka AK, Dhodapkar M, Burkeholder S, Taquet N, Rolland A, et al. Immune and clinical responses in patients with metastatic melanoma to CD34(+) progenitor- derived dendritic cell vaccine. Cancer Res 2001;61(17): 6451-6458.
e. Palucka AK, Dhodapkar MV, Paczesny S, Burkeholder S, Wittkowski KM, Steinman RM, et al. Single injection of CD34+ progenitor- derived dendritic cell vaccine can lead to induction of T-cell immunity in patients with stage IV melanoma. J Immunother 2003;26(5):432-439.
f. Bonifaz L, Bonnyay D, Mahnke K, Rivera M, Nussenzweig MC, Steinman RM Efficient targeting of protein antigen to the dendritic cell receptor DEC-205 in the steady state leads to antigen presentation on major histocompatibility complex class I products and peripheral CD8+ T cell tolerance. J Exp Med 2002;196(12):1627-1638. Disponible en http://www.ncbi. nlm.nih.gov/pmc/articles/PMC2196060/?tool=pubmed
g. Bonifaz LC, Bonnyay DP, Charalambous A, Darguste DI, Fujii SI, Soares H, et al. In vivo targeting of antigens to maturing dendritic cells via the DEC-205 receptor improves T cell vaccination. J Exp Med 2004;199(6):815-824.
La inmunoterapia de células dendríticas es uno de los tratamientos más publicados en los últimos 50 años, tanto a nivel de artículos científicos validados, reportes de los ciclos de ensayo y literatura de referencia (ver portadas de textos disponibles). Ya no existe duda de qué es, como funciona y para que aplica. La interrogante solo es: Que centros logran efectuar de mejor forma la práctica de dichos protocolos (similar interrogante a que cirujano opera mejor, que patólogo diagnóstica mejor, etc).

El Dr. Ider Rivadeneira, es un investigador comprometido con el avance de la medicina, Su perfil actual, destaca:
• Director de SOCHOM: Sociedad Chilena de Oncología Molecular.
• Director de SOCHIDEX: Sociedad Chilena de Inmunoterapia CD&EX.
• Médico acreditado en ARGENTINA: Matrícula Médico # 172373
• Médico acreditado en ECUADOR: Registro Salud de MSP No # 15332
• Médico acreditado en CHILE: Superintendencia de Salud # 385807
• Médico acreditado en ESPAÑA: Real Decreto # 285/2004- No# 2008/H09126.